|
艾滋病是全世界公共卫生的要紧威胁,据统计,全世界有约3800万人感染HIV-1病毒,抗逆转录病毒治疗(ART)很大程度上掌控了这些感染者的疾患发展,但没法根除身体的病毒,感染者必须终生用药,且容易受到药品毒性影响,并面临耐药危害。因此呢,找到一种没需ART就能达到缓解的疗法是征服艾滋病的下一步。
CAR-T细胞疗法是近年来一种备受关注的癌症免疫疗法,经过对T细胞进行基因工程改造,使其靶向清除特定癌细胞。基于这一原理,CAR-T细胞亦能够被改造用于识别和清除表达HIV-1病毒包膜糖蛋白(Env)的人类T细胞,从而用于治疗艾滋病。然而,迄今为止,还无一种抗HIV-1 CAR-T细胞能够长时间预防ART停药后的病毒反弹。这种没效的一个可能解释是显现了逃逸变异体,在接受单次抗HIV-1 CAR-T细胞治疗的HIV病人中观察到逃逸变异体。因此呢,扩大CAR识别以控制病毒逃逸,并使其靶向病毒储库,可能是研发用于治愈艾滋病的抗HIV-1 CAR-T细胞疗法的重要。
近期,复旦大学上海公共卫生临床中心徐建青科研员、张晓燕科研员、张仁芳专家医师,第四军医大学唐都医院孙永涛教授、广西中医药大学冷静教授等在 Cell Discovery 期刊发布了题为:Efficacy and safety of novel multifunctional M10 CAR-T cells in HIV-1-infected patients: a phase I, multicenter, single-arm, open-label study 的科研论文。
该科研研发了一种拥有三重功能的CAR-T细胞疗法——M10 CAR-T细胞疗法,包含对HIV-1感染细胞的广泛细胞毒性功效,中和隐藏其逆转后产生的游离病毒,以及B细胞滤泡归巢。科研团队还在18名HIV-1病毒感染者中进行了临床实验,结果表示,该CAR-T细胞疗法明显降低了病人的HIV-1 RNA水平,这些数据支持M10 CAR-T细胞做为治疗艾滋病感染者的新疗法的潜能。

联合广泛中和抗体(bNAb)是加强抗HIV-1 CAR-T细胞功能的一种有趣策略。CAR的功效依赖于识别表面表达的HIV-1病毒包膜糖蛋白(Env)表位,而bNAb能够经过直接阻断游离病毒与宿主细胞的结合来中和游离病毒,并经过与Fc受体结合来加强HIV-1特异性免疫应答。然而,针对这种二合一疗法应用于HIV感染者是不是能加强疗效,日前尚没探索。
另一方面,抗HIV-1 CAR-T细胞在身体表现的一个重要决定原因是它们的组织分布,更有效和更广泛的靶向病毒储库会带来更好的疗效。B细胞滤泡已被确定为慢性HIV-1感染时期隐藏和活性HIV-1的免疫特权避难所。科研显示,HIV-1特异性细胞毒性淋巴细在淋巴滤泡内累积失败是病毒连续复制的基本。趋化因子受体CXCR5被认为是驱动淋巴细胞迁移到B细胞滤泡的重要原因。与CXCR5的这一指点功效一致,在非人灵长类动物模型中,表达CXCR5的HIV-1特异性T细胞拥有强大的抗病毒活性,这显示靶向B细胞滤泡是研发更有效的抗HIV CAR-T细胞疗法的一种有前景的策略。
在这项新科研中,科研团队将以上策略结合在一块,研发了一种拥有三重功能的CAR-T细胞,这是一种携带内源性广泛中和抗体(bNAb)和滤泡归巢受体CXCR5的抗HIV-1 CAR-T细胞,科研团队将其叫作为M10细胞。M10细胞被设计为拥有三重生物学功能,包含对HIV-1感染细胞的广泛细胞毒性功效,中和隐藏其逆转后产生的游离病毒,以及B细胞滤泡归巢。
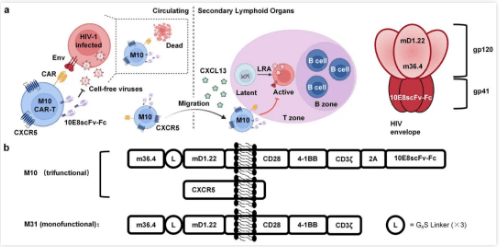
在证明了M10细胞的这种三重功能后,科研团队开展了一项针对HIV-1感染者的1期、多中心、单臂、开放标签的人体临床实验,共18名HIV-1感染者接受了间隔30天两次输注同种异体M10 细胞,每次输注M10细胞后,进行两次西达本胺刺激,以激活病人身体的HIV-1储存库,M10细胞输入明显控制了HIV-1病毒反弹,将血液中HIV-1病毒滴度峰值降低了74.3%,病毒载量平均下降了67.1%,10例病人在15天观察时期表示细胞关联HIV-1 RNA水平连续降低,还发掘M10细胞对隐藏的病毒储库施加选取性压力,科研中未观察到显著的治疗关联不良反应。
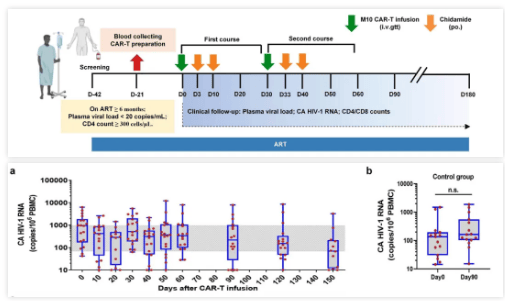
总的来讲,该科研支持了M10 CAR-T细胞做为一种新型、安全、有效的功能性治愈HIV-1感染或艾滋病的治疗选取的潜能。
本文链接:https://www.360worldcare.com/medical.article-4960-11.html返回外链论坛:http://www.fok120.com/,查看更加多
责任编辑:网友投稿
|