|

作者:Jerry
导读:癌症疫苗表示出在癌症预防和治疗方面巨大的潜能。然而,它们的疗效仍然受到限制,由于其免疫原性较弱,不可有效刺激细胞毒性T淋巴细胞(CTL)反应。
近期,中国药科大学莫然团队在期刊《Science Advances》 在线发布了题为“Lymph-targeted high-density lipoprotein-mimetic nanovaccine for multi-antigenic personalized cancer immunotherapy”的科研论文,该科研研发了一种高密度脂蛋白(HDL)模拟纳米疫苗,拥有淋巴靶向能力,能够利用脂质纳米颗粒有效诱导抗肿瘤免疫力,该脂质纳米颗粒共载有特定癌细胞膜携带的一系列肿瘤关联抗原和免疫佐剂。纳米疫苗的免疫接种控制了肿瘤的形成和生长,并明显加强了对小鼠模型中高干细胞性黑色素瘤的检测点控制剂的治疗效果。
https://www.science.org/doi/10.1126/sciadv.adk2444
科研背景
01
疫苗接种被认为是有效的预防传患病的干涉办法,可大大降低公共卫生中的发病率和死亡率。在过去的十年中,癌症疫苗得到了广泛的科研,其目的是经过肿瘤抗原特异性的细胞免疫反应来消除癌细胞。迄今为止,有些预防性疫苗已然被美国食品和药品管理局(FDA)准许,并用于预防乙型肝炎病毒和人乳头瘤病毒导致的恶性肿瘤。可是,肿瘤抗原的内源性特征是免疫原性低,常常很难诱导有效的免疫反应,这与来自外来病原体的抗原的传统疫苗有很大不同。
另外,传统疫苗诱导体液免疫,而由CD8+细胞毒性T淋巴细胞(CTLs)介导的细胞免疫在癌症疫苗杀死癌细胞中起着重要功效。经过应用全肿瘤裂解物、抗原与佐剂联合给药以及载体配方等多种策略,已然研发出多种加强疫苗效力的策略。纳米载体被认为是癌症疫苗有前景的递送载体,它有助于将抗原定向递送至重要免疫器官和细胞类型。继发性淋巴器官,尤其是淋巴结(LNs),饱含树突状细胞(DCs)和T细胞,这些细胞是癌症疫苗强抗原特异性CTL介导反应的重要靶点。针对LNs和DCs的有效递送系统仍然是研发癌症疫苗的理想选取。
科研发展
02
科研人员首要在黑色素瘤预防模型上评定了R837/LNP-M-L的身体抗肿瘤功效,小鼠在尾基部皮下接种了不同LNP疫苗,包含R837/LNP-L、R837/LNP-M、LNP-M-L和R837/LNP-M-L,间隔1周接种3次,最后一次接种后7天,小鼠被皮下移植B16F10 ACs,并监测其肿瘤形成和生长状况。接种R837/LNP-M-L的延迟肿瘤形成效果最好,表现为肿瘤生成速度最慢,形成的肿瘤体积最小。
接下来,科研人员评定了R837/LNP-M-L在控制高干性黑色素瘤形成和发展中的预防效果。科研结果显示,R837/LNP-M-L是一种有效的癌症疫苗,可控制黑色素瘤的出现和发展,并经过配备不同表型黑素瘤细胞的细胞膜,实现了针对不同恶性程度黑素瘤包含高干性黑素瘤的个性化免疫。
科研人员进一步探索了R837/LNP-M-L抗肿瘤的机制。结果显示R837/LNP-M-L疫苗克服了肿瘤的免疫控制微环境,经过增多肿瘤和淋巴结内CD8+ T细胞的频率,从而加强了与aPD1联合的治疗效果。
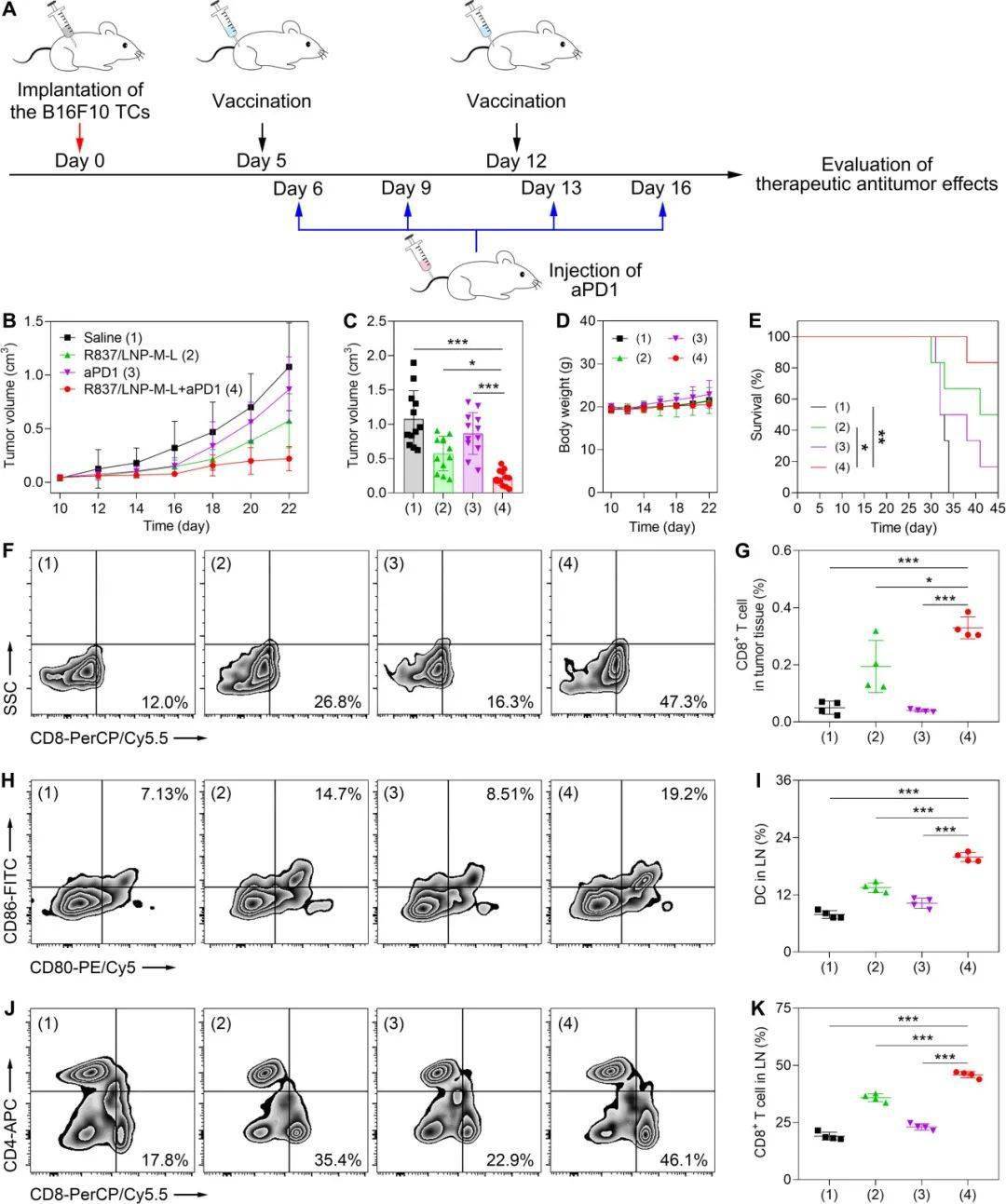
R837/LNP-M-L对csc富集的黑色素瘤小鼠模型的治疗性抗肿瘤功效
科研结论
03
接种R837/LNP-M-L延缓了黑色素瘤小鼠模型的肿瘤形成和生长,并加强了临床应用的免疫检测点控制剂对干细胞性免疫耐药性黑色素瘤的治疗效果。
参考资料:
https://www.science.org/doi/10.1126/sciadv.adk2444
注:本文旨在介绍医学科研发展,不可做为治疗方法参考。如需得到健康指点,请至正规医院就诊。
热门·直播/活动
|