|
近期,国家药物监督管理局(NMPA)官网表示,经过优先审评审批程序准许Bristol-Myers Squibb Company申报的1类创新药瑞普替尼胶囊(商品名:奥凯乐/AUGTYRO)上市,适用于ROS1阳性的局部晚期或转移性非小细胞肺癌(NSCLC)成人病人。

2023年5月,瑞普替尼在华的上市申请获受理,并得到优先审评资格(详情链接:瑞普替尼上市在即!针对ROS1阳性非小细胞肺癌获CDE和FDA优先审评)。另外,该适应症已于2023年11月16日获美国FDA准许上市(详情链接:瑞普替尼美国上市!用于治疗ROS1阳性的局部晚期或转移性非小细胞肺癌成人病人)。


瑞普替尼获准依据
这次获准是基于全球性、多中心、单臂、开放标签、多队列的I/II期TRIDENT-1临床科研(NCT03093116)结果。
科研设计
TRIDENT-1旨在评定瑞普替尼在晚期实体瘤( 包含NSCLC )病人中的安全性、耐受性、药代动力学和抗肿瘤活性,I/II期包含拥有ROS1融合的局部晚期或转移性实体瘤病人。实验的第1周期包含剂量递增,以确定第二周期的举荐剂量。该实验的II期重点终点为客观缓解率 ( ORR )。重要次要终点包含6个不同扩展队列( 包含TKI初治和经治的ROS1阳性局部晚期或转移性NSCLC病人 )中按照实体瘤疗效评估标准( RECIST v1.1 )评定的缓解连续时间( DOR )、没发展存活期( PFS )和颅内缓解。
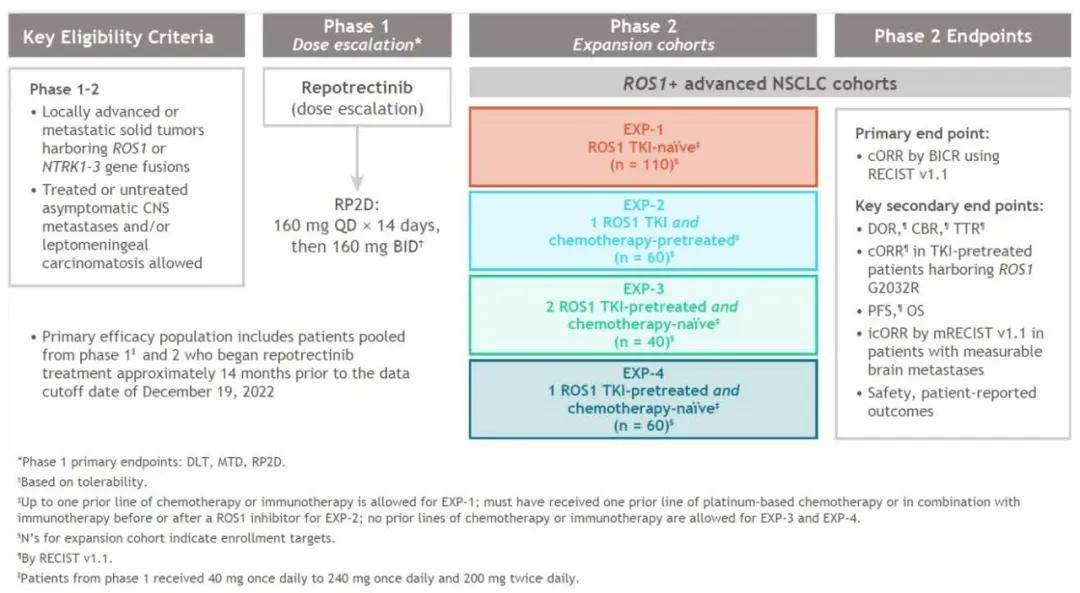
▲科研设计
科研结果
TRIDENT-1科研结果表示,在TKI初治病人(n=71)中,客观缓解率(ORR)为 79% ,其中10%的病人显现完全缓解( CR ),69%的病人显现部分缓解( PR )。中位随访时间为24.0个月( 范围,14.2-66.6 ),中位缓解连续时间( mDOR )为34.1个月, 中位没发展存活时间为35.7个月( 95%CI,27.4-没法估计 )。
在TKI经治病人中,38%( 95% CI:25-52 )( N=56 )对治疗有反应,5%显现CR,32%显现PR,中位随访时间为21.5个月( 范围,14.2-58.6 ),mDOR为14.8个月( 95%CI,7.6-没法估计 ),中位没发展存活时间为9.0个月( 95%CI,6.8-19.6 )。
在基线时拥有可测绘脑转移的病人中(仅在第二周期实验中) ,9例既往未接受过ROS1控制剂治疗,其中有8例得到了颅内缓解( 89%;95%CI,52-100 );而在13例既往接受过一次ROS1控制剂但未接受过化疗的病人中,有5例得到了颅内缓解( 38%;95%CI,14-68 )。
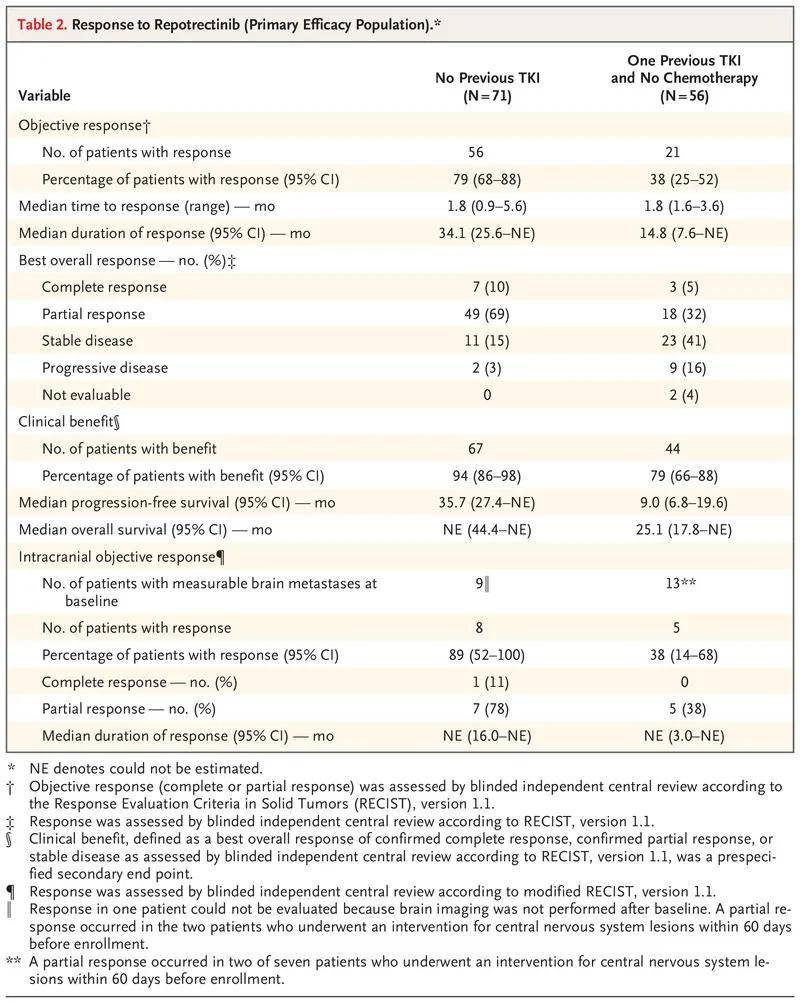
▲TRIDENT-1科研中ROS1阳性NSCLC病人的疗效数据
并且针对经治、携带ROS1 G2032R病人(N=17),ORR为59%( 1例CR,9例PR )。

▲科研结果-ROS1 G2032R亚组
瑞普替尼
瑞普替尼是靶向功效于包含非小细胞肺癌在内的晚期实体瘤ROS1和NTRK致癌因子的新一代激酶控制剂。携带ROS1和NTRK基因融合的肿瘤病人在接受日前已获准准的靶向治疗后,一般会显现耐药突变,这些突变限制了药品与靶点的结合,最后引起肿瘤发展。瑞普替尼是第二代靶向ROS1或NTRK阳性局部晚期或转移性实体瘤的新型TKI,旨在加强缓解率并延长缓解时间,并拥有良好的颅内活性。

▲ROS1基因结构和信号通路
在NSCLC病人中,ROS1基因融合占比仅为1%-2%,但因为肺癌发病率高,ROS1阳性NSCLC病人体量不可小觑。2024年CSCO非小细胞肺癌诊疗指南中指出:ROS1融合阳性IV期NSCLC一线治疗Ⅰ级举荐应用克唑替尼和恩曲替尼 ,Ⅲ级举荐应用瑞普替尼。另外 2024v5版非小细胞肺癌NCCN指南举荐 克唑替尼(优先举荐)、恩曲替尼(优先举荐)、 瑞普替尼(优先举荐)和塞瑞替尼用于ROS1融合阳性的NSCLC病人的一线治疗。针对脑转移病人,恩曲替尼和瑞普替尼疗效更好。

▲2024年CSCO非小细胞肺癌诊疗指南

▲2024v5版非小细胞肺癌NCCN指南
参考文献:
[1]再鼎医药官网.
[2]百时美施贵宝官网.
[3]瑞普替尼说明书.
[4]NMPA、CDE官网.返回首页,查看更加多
外链论坛:http://www.fok120.com/
|